Programme de développement :
Viaskin™ Milk
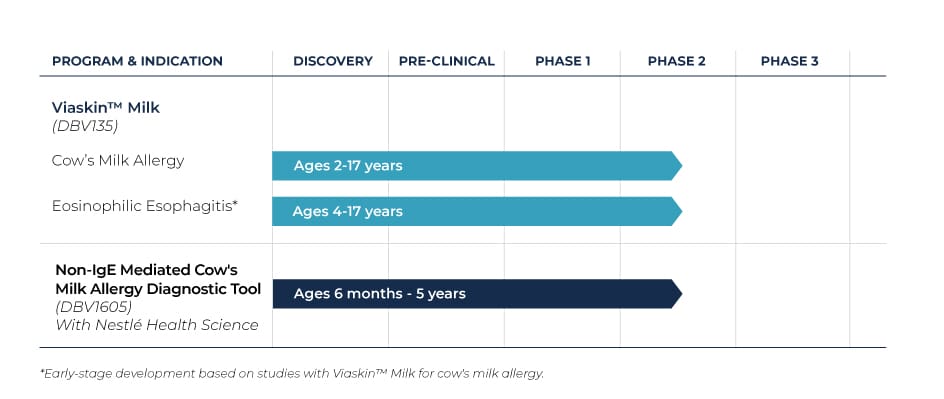
L’allergie aux protéines de lait de vache (APLV) est souvent la première allergie à apparaître chez le nourrisson. Elle affecte environ 2 à 3 % de la population dans les pays développés.
Nous avons terminé un essai clinique de phase 1/2 pour étudier la sécurité et l’efficacité chez des patients pédiatriques et adolescents.
Essais cliniques (allergie au lait de vache IgE médiée)
MILES (Viaskin® Milk efficacité et sécurité)
MILE est un essai clinique de Phase 1/2, randomisée, en double aveugle, et contrôlé par placebo, destiné à étudier la sécurité et l’efficacité de Viaskin® Milk chez des patients souffrant d’allergie aux protéines de lait non IgE-médiée, ou APLV. L’essai multicentrique a été mené dans 17 sites en Amérique du Nord. L’étude a été divisée en deux parties consécutives. La partie A de l’étude MILES est terminée et n’a pas révélé de problème de sécurité. La partie B a été conçue pour déterminer une dose sûre et efficace au sein de deux groupes d’âge: des enfants âgés de 2 à 11 ans et des adolescents âgés de 12 à 17 ans.
Collaborations externes
Essai clinique pilote d’immunothérapie épicutanée dans l’allergie au lait de vache avec l’Assistance Publique Hôpitaux de Paris (AP-HP)
En 2006, un essai clinique pilote en double aveugle, contrôlé par placebo a été initié avec l’AP-HP pour évaluer la sécurité de Viaskin® Milk chez les enfants souffrant d’une allergie au lait de vache. L’essai pilote a inclus 21 nourrissons (à partir de 3 mois) et enfants (jusqu’à l’âge de 15 ans).
En savoir plus
Essais cliniques (diagnostic d’allergie au lait IgE médiée)
APTITUDE
APTITUDE est un essai clinique de Phase 2 non randomisé en triple aveugle, contrôlé par placebo. L’essai est conduit dans 27 sites en Amérique du Nord et en Europe. Cette étude, à deux bras, est conçue pour évaluer la sensibilité, la spécificité ainsi que la valeur prédictive positive et négative de DBV1605 comme patch test épicutané d’atopie, prêt à l’emploi, pour le diagnostic d’une allergie au lait de vache non-IgE médiée chez les enfants âgés de 1 mois à 5 ans. Il s’agit d’un essai en cours incluant environ 230 sujets.
En savoir plus
*Viaskin® Milk est un produit expérimental dont l’utilisation n’a été approuvée dans aucun pays quel qu’en soit l’usage.
